美國非牟利組織Public Health and Medical Professionals for Transparency (PHMPT)早前獲得一批美國食品藥品監督管理局(FDA)有關復必泰疫苗的數據及文件,並上載至其網站公開。不少本地及海外網民引用其中一份報告的資料,指復必泰疫苗的副作用多達1,291種,列出來長達9頁,又表示接種疫苗後獲不良反應的比例驚人。傳真社查看報告原文,發現該1,291種不良反應的列表只是監察清單,而非實際出現的疫苗副作用列表,而且不少帖文錯誤引用文中數據,包括將呈報個案數目當作總接種人數來計算,誇大了接種風險。
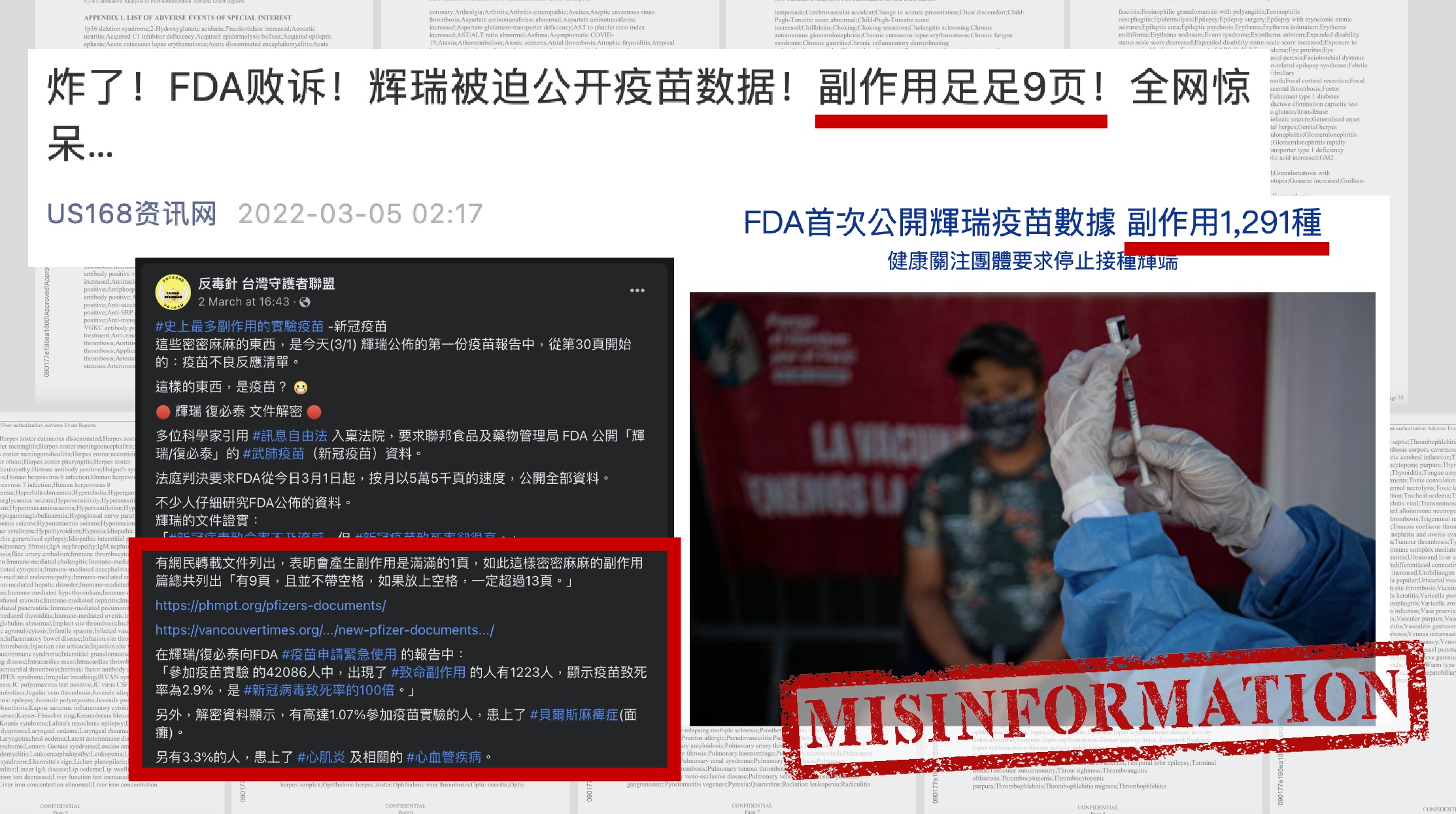
該份載有千種「副作用」的文件是輝瑞藥廠向FDA申請註冊藥劑(biologics license application)時提交的疫苗安全數據分析報告,題為「5.3.6 Cumulative Analysis of Post-authorization Adverse Event Reports of PF-07302048 (BNT162B2) received through 28-Feb-2021」。報告包括一份9頁的附件,列出過千種不良反應的醫學名稱。網上一則廣傳訊息引用該附件指「輝瑞被迫公開疫苗數據!副作用足足9頁!」,《大紀元》亦於3月5日發布「FDA首次公開輝瑞疫苗數據 副作用1,291種」報道,指文件提到輝瑞疫苗1,291種副作用包括腎臟損傷、心臟出血性腦炎等。
不過,該份9頁的附件標題註明,它實為復必泰疫苗的關注事件(Adverse Event of Special Interest, AESI)列表,並非副作用列表。根據世界衛生組織指引,AESI是指預先被辨認及定義、有可能與疫苗有因果關係的嚴重醫學事件,需在未來小心監察及研究。(A preidentified and predefined medically-significant event that has the potential to be causally associated with a vaccine product that needs to be carefully monitored and confirmed by further specific studies.)
AESI與疫苗接種後的異常事件(Adverse Event Following Immunization, AEFI)不同。按世界衛生組織定義,AEFI是接種疫苗後發生的任何異常醫學事件,亦即由接種了疫苗的人士呈報的各種不良反應。相反,AESI列表是一張預先定義可能與疫苗有關的事件清單,供研究人員持續監察疫苗是否會引致該些不良反應。
預先列出的AESI不一定會發生為AEFI,而已發生的AEFI亦不一定包括在AESI列表之中。報告中研究方法部分提到,輝瑞將由2020年12月1日至2021年2月28日接獲的自願通報異常事件(adverse event)個案組成一個資料庫,並根據此資料庫的數據分析疫苗安全性。報告第3.1.3節正正按著資料庫中的異常事件個案分類,分析它們是否屬於任何一類AESI。例如心血管疾病本來已被列為其中一類AESI,報告分析輝瑞資料庫共42,086宗異常事件個案中有1,403宗與心血管疾病有關,認為結果沒有揭示疫苗安全性方面的新發現,但之後仍會繼續監察情況。
報告又提到,這些個案來自醫學文獻、臨床試驗及由政府衛生部門呈報等,但由於是自願呈報,資料或未夠準確及全面,部分個案亦缺乏患者病史及接種疫苗的詳情,因此,在報告列出的異常事件不一定由疫苗引發。
除誤解AESI為已出現的副作用外,數據亦被錯誤引用。Facebook專頁「反毒針 台灣守護者聯盟」的一則帖文稱「參加疫苗實驗的42,086人中,出現了致命副作用的人有1,223人,顯示疫苗致死率為2.9%」,但報告所列並非一場「實驗」的數據,而是由各方呈報的個案。42,086實為輝瑞接獲異常事件個案總數,當中1,223宗為致命(fatal)事件。由於42,086只是呈報異常事件的個案數量,不是接種疫苗的總人數,所以不能作為計算「疫苗致死率」的基數,帖文所指的2.9%並無根據。
「反毒針 台灣守護者聯盟」的帖文又因將42,086當作為實驗人數,錯指有1.07%參加疫苗實驗的人出現面癱、3.3%患上心肌炎及心血管疾病、8.5%患上自身免疫性疾病等,令人以為這些是接種復必泰疫苗的患病風險。不過,由於基數是異常事件的總數,這些只是各種不良反應佔接獲異常事件總數的比例。
由科學家、傳媒、公共衛生及醫學專家等人組成的PHMPT早前按美國《自由資訊法》要求美國食品藥品監督管理局(FDA)提供有關輝瑞/復必泰疫苗的所有研究數據及資料。FDA解釋資料繁多,需時55年才能整理及公開所有數據。PHMPT後於去年9月入稟德州法院,要求FDA加快公開進度,法院指由於資料涉及重大公眾利益,裁定FDA須在8個月內公開所有文件。PHMPT將其陸續取得的文件及數據上載至其網站供公眾查閱,本文所指的報告為網站現時已公開的150份文件的其中一份。
該份輝瑞呈交FDA的報告封面顯示,報告於2021年4月30日獲批。復必泰疫苗首先於2020年12月2日獲准在英國作緊急用途,美國FDA後於2021年8月23日宣布批准16歲及以上人士接種。
傳真社向《大紀元》查詢及在「反毒針 台灣守護者聯盟」的帖文留言,告知內容有誤,詢問會否因此更正或刪除報道或帖文。《大紀元》將「副作用」字眼改為「不良事件」,「反毒針 台灣守護者聯盟」則未有回覆。
輝瑞向FDA提交的疫苗安全數據分析報告
—————————————————
傳真社經fact check將內容分作以下3類:
Fake News (假新聞):以新聞形式發布的造假消息
Disinformation (虛假資訊):發布不實資訊
Misinformation (誤傳資訊):發布的資訊內容有錯誤
—————————————————
資料來源:
輝瑞向FDA提交的疫苗安全數據分析報告:5.3.6 Cumulative Analysis of Post-authorization Adverse Event Reports of PF-07302048 (BNT162B2) received through 28-Feb-2021
https://phmpt.org/wp-content/uploads/2021/11/5.3.6-postmarketing-experience.pdf
PHMPT公開文件網站
https://phmpt.org/pfizers-documents/
世界衛生組織指引:Establishing active surveillance systems for adverse events of special interest during COVID-19 vaccine introduction
https://www.who.int/vaccine_safety/committee/Module_AESI.pdf
香港衛生署簡報:新冠疫苗接種異常事件的監察
https://www.covidvaccine.gov.hk/pdf/monitoring_of_AEFI_brief_bilingual.pdf
網傳文章:炸了!FDA敗訴!輝瑞被迫公開疫苗數據!副作用足足9頁!全網驚呆…
https://mp.weixin.qq.com/s/9C0ETAd9IOPTRMzZjDu1Tw
《大紀元》:FDA首次公開輝瑞疫苗數據 副作用1,291種
https://www.epochtimes.com/b5/22/3/5/n13623663.htm
Facebook專頁「反毒針 台灣守護者聯盟」帖文
https://www.facebook.com/taiwanguardians/posts/144221611412365
https://www.facebook.com/taiwanguardians/posts/146123304555529
Instagram帳戶「anti_green_pass_hk」帖文
https://www.instagram.com/p/Ca4gjMuPPgY/
路透社就同一文件的Fact Check報道
https://www.reuters.com/article/factcheck-pfizer-documentpregnant-idUSL1N2U81ZL
法新社就同一文件的Fact Check報道
https://factcheck.afp.com/http%253A%252F%252Fdoc.afp.com%252F9UC4LE
「求驗傳媒」就相關帖文的Fact Check報道
https://www.facebook.com/kauyim/posts/4867183563357820